近期,国际权威期刊 《Molecular Biomedicine》(IF 10.1)上刊载了由海军军医大学第三附属医院(东方肝胆外科医院)沈锋、杨田教授团队、联合吉林大学第一医院、天津市第三中心医院和鹍远生物(Singlera Genomics) 等的重要研究成果:“Development and validation of a high-confidence diagnostic model integrating ctDNA methylation and serum biomarkers for early-stage hepatocellular carcinoma detection(整合ctDNA甲基化与血清生物标志物的高置信度诊断模型用于早期肝细胞癌检测的研发与验证)[1]”。该研究证实了鹍远生物的肝癌多基因甲基化检测(HepaAiQ®,甘艾克®)在早期肝细胞癌的检出性能显著优于现有常见的血清学标志物(如AFP、DCP、AFP-L3等)。在此基础上,该研究开发了结合HepaAiQ®甲基化评分、AFP、DCP及年龄、性别等在内的GAMAD多维度肝癌早诊模型,并在与国际公认的GALAD模型头对头比较中全面胜出,对BCLC 0-A期早期肝细胞癌(HCC)的检出敏感性达到83.9%,显著优于西方标准模型。
据公开资料显示,肝细胞癌是全球癌症死亡的第三大原因,而中国承担着全球近一半的肝癌负担。与欧美以酒精性和脂肪性肝病为主不同,我国超过80% 的肝癌与乙型肝炎病毒(HBV)感染相关。这一根本性的病因学差异,导致基于西方人群开发的诊断模型在中国人群中的应用效能受到显著影响。以国际广泛使用的GALAD模型为例,其虽较单一甲胎蛋白(AFP)有所改进,但在HBV高流行人群中的诊断性能仍存在明显局限。临床亟需一种更契合中国病因学特点、更精准的早诊工具——这不是对现有模型的简单优化,而是需要针对中国人群特征进行重新构建。
正是源于这一临床痛点,研究团队与鹍远生物展开深度合作,将新型的血液ctDNA甲基化检测与临床结合,孕育出GAMAD这一中国方案。“从单一标志物到多组学融合,我们希望通过技术创新,真正解决中国肝癌高危人群的早诊难题。”杨田教授表示。
本研究采用的ctDNA甲基化检测技术(HepaAiQ®),系复旦大学附属中山医院周俭院士牵头、联合鹍远生物等多家单位共同申报的“国家重点研发计划-重大慢性非传染性疾病防控研究专项:基于液体活检技术的常见恶性肿瘤筛查及早诊技术研发与评价研究”的核心成果之一。该技术于2024年已在国际权威期刊《Clinical and Translational Medicine》发表了早期研发成果,验证检测技术在肝癌早期检测与预后评估的临床价值[2]。本次多中心前瞻性中国肝癌高危人群的早诊GAMAD模型的成功,是继鹍远生物HepaAiQ®技术获得欧盟CE认证后,在临床应用转化中的又一里程碑。
【研究设计】
该研究设计了多阶段、多中心的严谨验证流程(图1):首先评估单个生物标志物的诊断性能,进而构建多因素诊断模型,最后在独立测试集中验证模型效能。
第一阶段:单标志物性能评估。研究团队在1,692例受试者(包括476例HCC患者和1,216例对照)中,系统比较了HepaAiQ® ctDNA甲基化检测与传统血清标志物AFP、AFP-L3、DCP的诊断性能。
第二阶段:多因素模型构建。基于单标志物评估结果,团队筛选出最优变量组合,在训练集中构建了整合性别、年龄、HepaAiQ®甲基化评分、AFP、DCP五个维度的GAMAD模型,并在验证集中进行内部验证。
第三阶段:独立测试验证。在独立的测试集(含158例HCC患者和407例对照)中,对GAMAD模型的诊断效能进行最终验证,并与国际主流GALAD模型进行“头对头”比较。
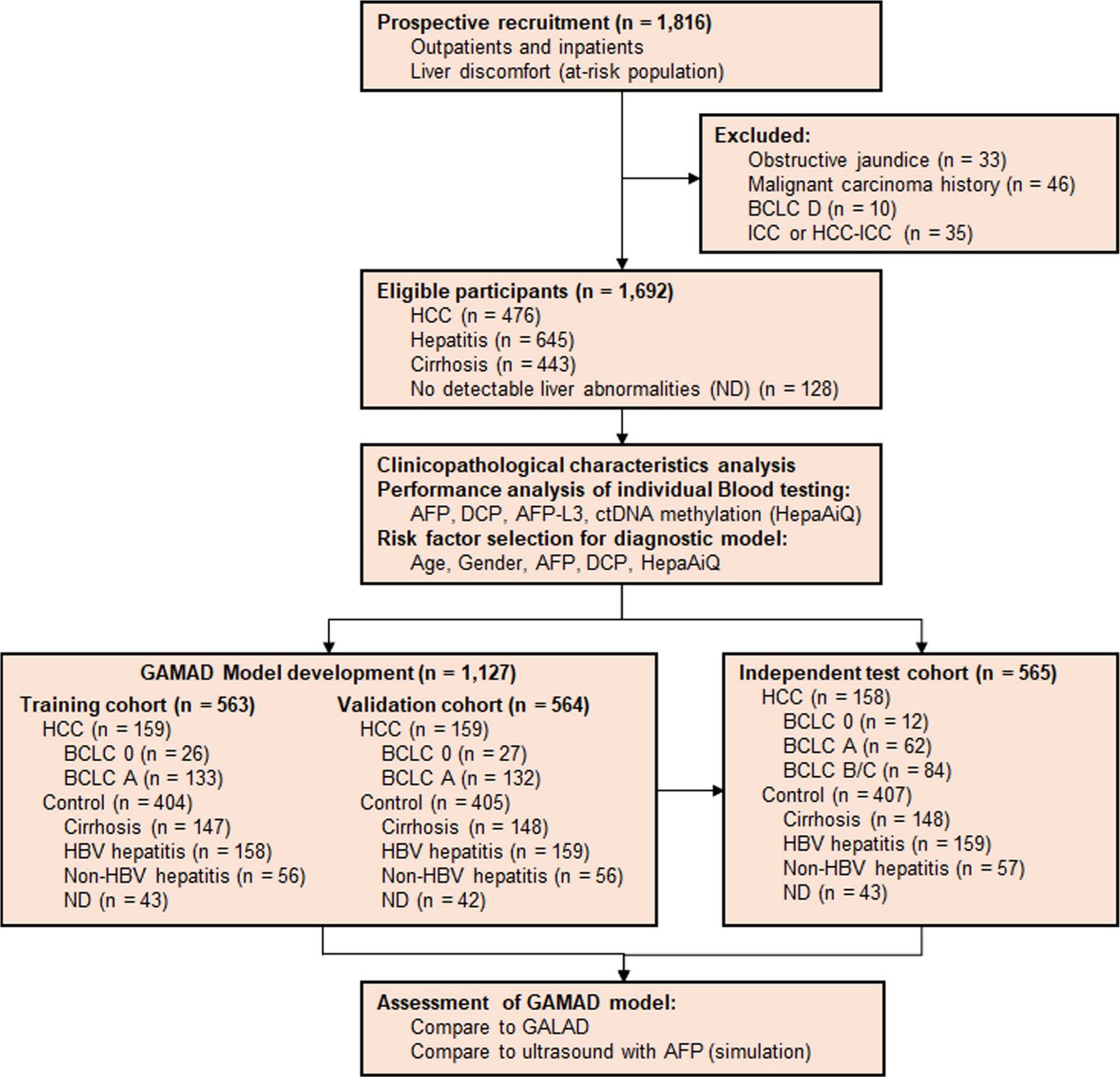
图1. 研究设计示意图
【结果】
本研究共纳入1,692例受试者,包括476例肝细胞癌(HCC)患者和1,216例对照(645例肝炎、443例肝硬化、128例无肝异常者)。HCC患者中BCLC 0/A期占82.4%(392/476),BCLC B/C期占17.6%(84/476)。研究将66.6%(1,127例)患者用于模型开发(分为训练集和验证集),剩余33.4%(565例)作为独立测试集。
单标志物性能比较:在单标志物性能比较中,HepaAiQ® ctDNA甲基化检测表现出显著优势。HepaAiQ®对BCLC 0-A期早期肝癌的敏感性达71.2%,显著高于传统血清标志物AFP(45.4%)、DCP(47.2%)和AFP-L3(31.6%)。其整体诊断AUC为0.862,同样优于AFP(0.761)、AFP-L3(0.708)和DCP(0.839)(P < 0.001)。更关键的是,在AFP、DCP和AFP-L3均为阴性的HCC患者中,HepaAiQ®仍能检出56.2%。
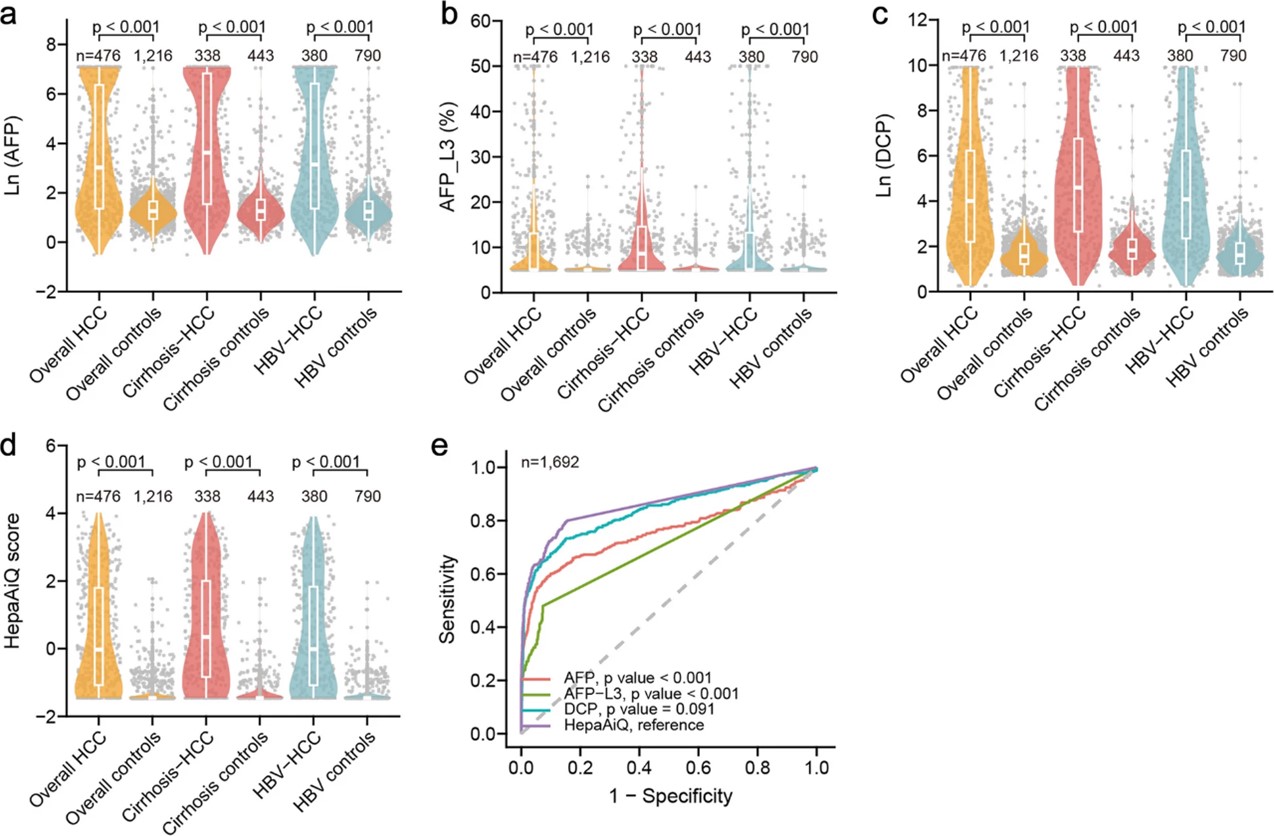
图2. 血清肿瘤标志物与HepaAiQ®的性能表现。
GAMAD模型构建与验证:基于单因素和多因素回归分析,研究团队在训练集中构建了整合性别、年龄、HepaAiQ®甲基化评分、AFP、DCP五个维度的GAMAD模型。在训练集中,GAMAD模型对早期HCC的AUC达0.948,敏感性86.2%,特异性90.3%。在验证集中,GAMAD对BCLC 0-A期HCC的敏感性为80.5%,特异性90.4%,AUC为0.934(95% CI: 0.911-0.957)。在独立测试集中,GAMAD对BCLC 0-A期HCC的敏感性达86.5%,对BCLC B-C期HCC达91.7%,AUC为0.952(95% CI: 0.931-0.973)。
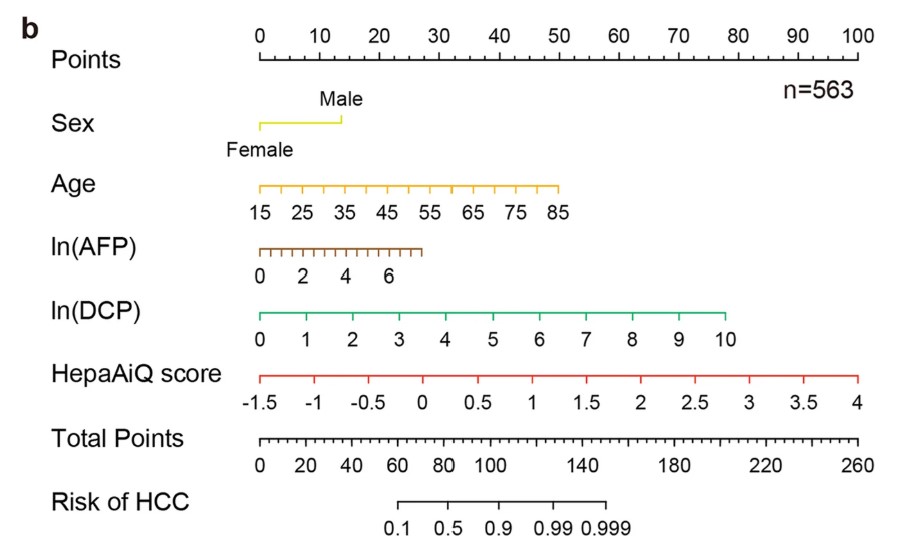
图3. 早期肝细胞癌诊断模型“GAMAD”的建立。
头对头对比GALAD模型: 与国际公认的GALAD模型进行“头对头”比较,GAMAD在三个队列中均表现更优(图4):训练集AUC 0.948 vs 0.899,验证集0.934 vs 0.906,测试集0.952 vs 0.926。在GALAD误判为阳性的208例对照中,GAMAD成功纠正了114例(54.8%);在GALAD漏诊的HCC患者中,GAMAD仍能检出40.2% GAMAD较GALAD的净重新分类指数(NRI)为0.959(P < 0.001),综合判别改善指数(IDI)提升0.087(P < 0.001),决策曲线分析显示平均净收益提升18.9%。
亚组分析显示,在HBV相关肝癌这一中国核心病因人群中,GAMAD的AUC高达0.954(95% CI: 0.941-0.966),显著高于GALAD的0.914(P < 0.001)。在肝硬化亚组中,GAMAD的AUC为0.941,优于GALAD的0.902(P < 0.001);在非HBV亚组中,GAMAD的AUC为0.917(P < 0.001),同样显著优于GALAD的0.897(P < 0.001)。此外,在HBV患者中,接受抗病毒治疗者(AUC 0.945)与未治疗者(AUC 0.958)的GAMAD性能无显著差异(P = 0.311),表明抗病毒治疗不影响模型诊断效能。
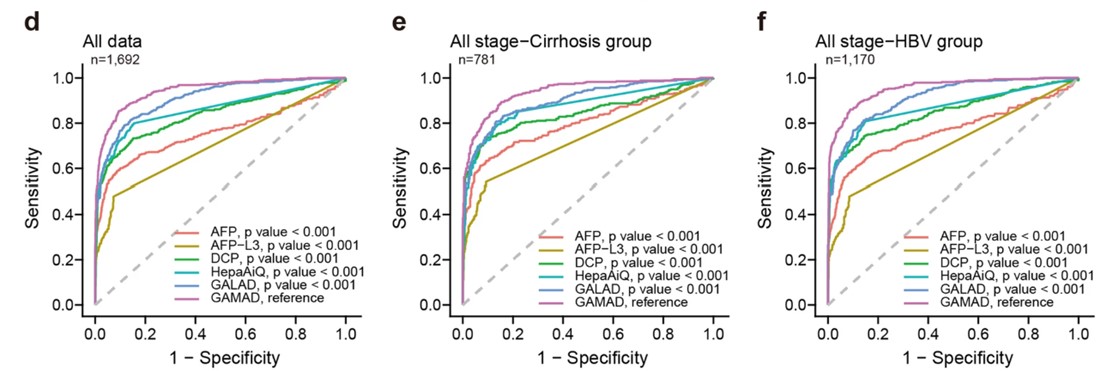
图4. GAMAD模型性能比较。
人群筛查模拟:在10万高危人群的蒙特卡洛模拟中,GAMAD较传统“超声+AFP”方案多检出早期肝癌约1,600例(从1,030例增至2,630例),阳性预测值从15.1%提升至28.0%,假阴性率从37.2%降至16.3%。
【结语】
本研究通过中国肝癌高危人群的前瞻性验证了一系列可应用于临床检测的经济高效、易于操作的方法,包括新型的分子检测技术- HepaAiQ®(ctDNA甲基化检测),并在此基础上构建了整合临床与血液检测的最优变量的GAMAD多维度诊断模型。研究发现,HCC患者血浆中的特定ctDNA甲基化模式在早期检测中性能卓越,HepaAiQ®单独应用时敏感性和特异性均优于传统血清标志物AFP和DCP;而GAMAD模型的构建,更将诊断效能提升至全新高度——在与国际公认的GALAD模型“头对头”对决中全面胜出,对早期肝癌的检出敏感性达83.9%,特异性达90.4%,在HBV相关肝癌这一中国核心病因人群中AUC高达0.954。
这是肝癌早诊早治的临床应用转化的重要里程碑,标志着自主研发的检测技术与顶尖临床资源的深度“产学研医”合作,成功孕育出针对中国肝癌高发人群量身定制的早诊“中国方案”。
这种ctDNA检测方法不仅有助于进一步提升HCC患者的早期诊断率,更有望为高危人群的预防性筛查和疗效监控提供一个更便捷、更精准的临床工具。从HepaAiQ®到GAMAD,鹍远生物将继续深耕甲基化液体活检领域,推动更多创新技术从实验室走向诊室,让精准、可及的“中国方案”惠及中国亿万肝癌高危人群,为全球肝癌防控贡献中国力量。
【参考文献】
[1] Wu H, Wang MD, Wan ZY, Yao LQ, et al. Development and validation of a high-confidence diagnostic model integrating ctDNA methylation and serum biomarkers for early-stage hepatocellular carcinoma detection. Molecular Biomedicine, 2026.
[2] Guo DZ, Huang A, Wang YC, Zhou S et al. Early detection and prognosis evaluation for hepatocellular carcinoma by circulating tumour DNA methylation: A multicentre cohort study. Clinical and Translational Medicine, 2024.
免责声明:*本文仅供医学专业人士阅读参考,非广告用途。医学界力求其发表内容专业、可靠,但不对内容的准确性做出承诺;请相关各方在采用或以此作为决策依据时另行核查。本平台所有原创内容,未经书面授权,任何单位及个人不得转载,我们保留追究法律责任的权利。转载与合作请联系info@singleragenomics.com。





